GS1-01.阿贝西利联合辅助内分泌治疗(abemaciclib+ET)用于高危早期乳腺癌的monarchE研究主要终点(PO)无浸润性疾病生存(iDFS)结果分析
monarchE是一项随机、开放标签的多中心Ⅲ期临床研究,旨在比较abemaciclib+标准内分泌治疗和单纯标准内分泌治疗对于HR+/HER2-高危早期乳腺癌患者的疗效和安全性。该研究共从38个国家600多个中心纳入了5637例患者,按1:1比例分别随机abemaciclib+标准内分泌治疗或单纯标准内分泌治疗(ET)。入组患者病理腋窝淋巴结(ALN)阳性≥4个,或阳性腋窝淋巴结数为1至3个且至少具有以下一种高风险特征:原发性浸润性肿瘤≥5cm;肿瘤组织学分级3级;或中心实验室检测的Ki67指数≥20%。并根据既往是否接受化疗,患者绝经状态和地区进行分层。
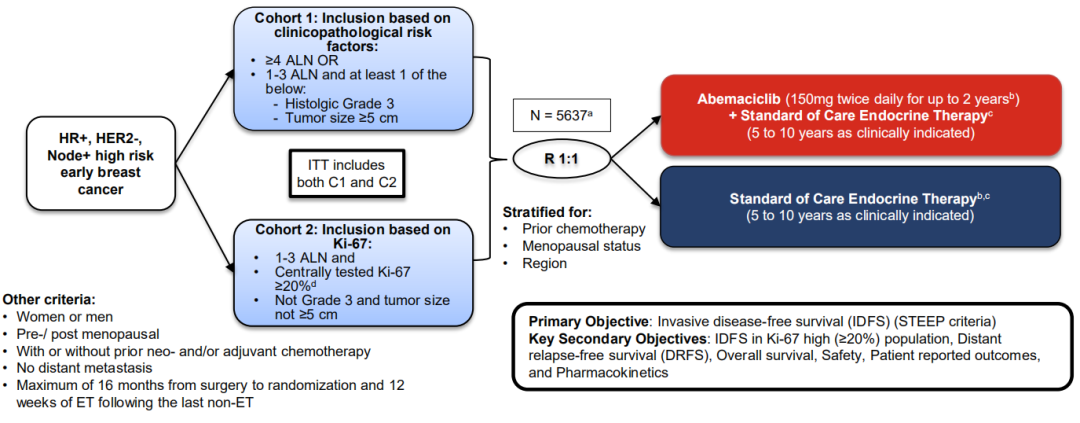
主要研究终点为基于“疗效终点标准定义”(STEEP)标准的iDFS。次要研究终点包括:无远处复发生存期(DRFS)、Ki67高表达人群的iDFS、总生存期(OS)、安全性、药代动力学。
2020年SABCS大会上公布了monarchE研究主要终点iDFS的最终分析结果。中位随访时间为19.1个月,该研究达到预期主要终点,共有395例iDFS事件例数发生(预期为390例),具有统计学意义。

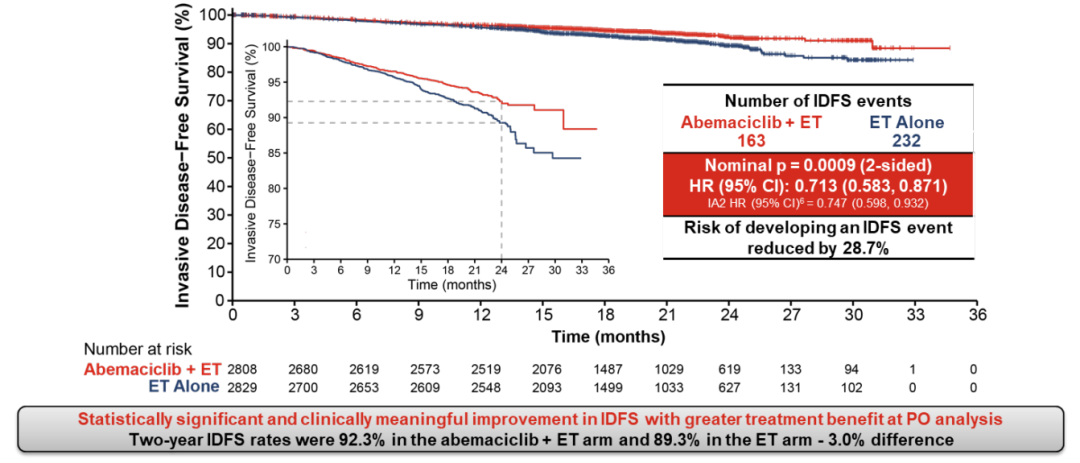
ITT人群中,iDFS的主要终点分析显示,abemaciclib+ET组与ET组相比,iDFS风险降低28.7%(HR 0.713,95%Cl:0.583~0.871),有统计学意义和临床意义的改善,2年iDFS率提高3.0%(阿贝西利组为92.3%,对照组为89.3%),提示其具有更大的治疗效益。
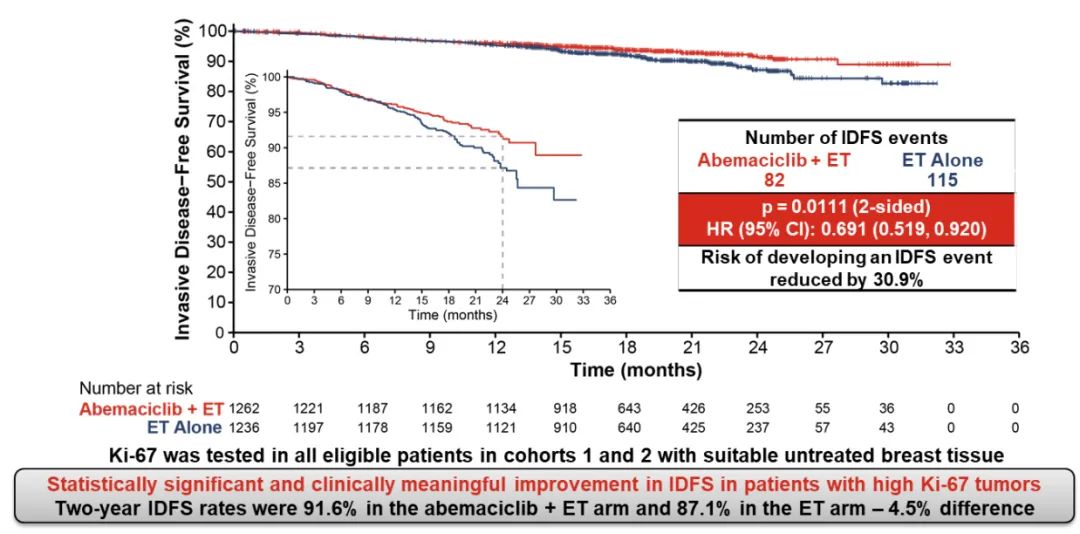
在高Ki67(≥20%)的肿瘤患者中,iDFS事件数量在abemaciclib+ET组为82,ET组为115(HR 0.691,95%Cl:0.519~0.920 P=0.0111),在abemaciclib的治疗下,iDFS事件风险降低30.9%,具有统计学意义和临床意义。abemaciclib+ET两年iDFS发生率为91.6%,ET组为87.1%,组间差异为4.5%。
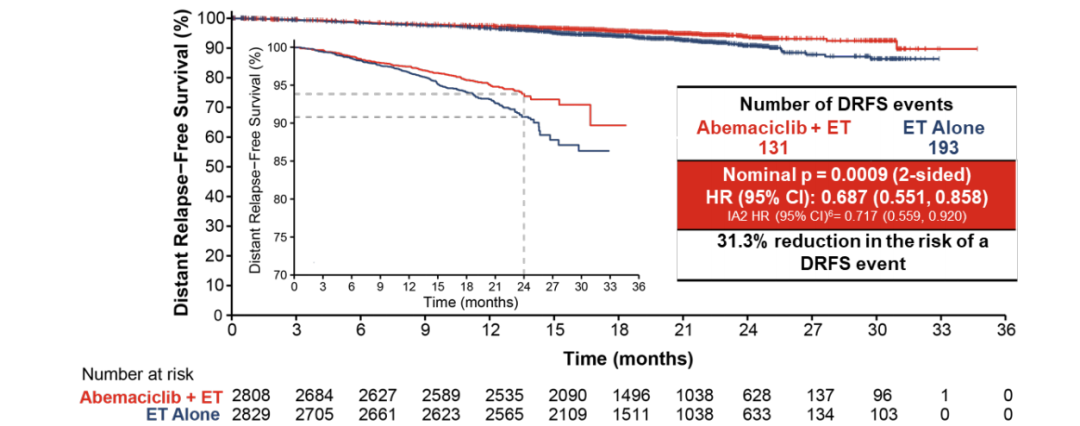
ITT人群中,abemaciclib+ET组DRFS事件数量为131,ET组为193(HR 0.687,95%Cl:0.551~0.858 P=0.0009),在abemaciclib的治疗下DRFS事件风险降低31.3%,abemaciclib+ET组两年DRFS发生率为93.8%,ET组为90.8%,组间差异为3.0%。DRFS风险的降低具有临床意义和治疗意义。
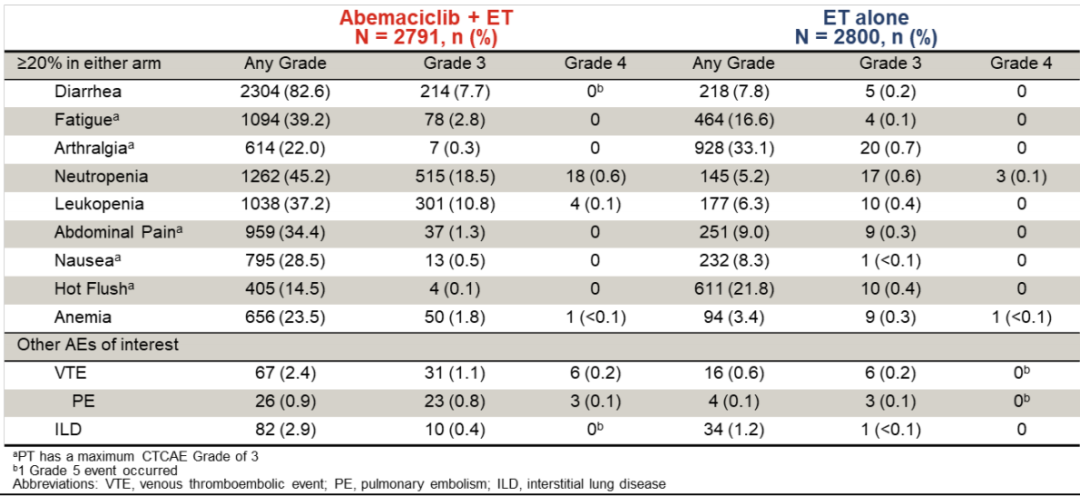
安全性与已知的第二次中期分析结果一致,腹泻、疲劳是主要表现。
2020年9月,monarchE研究的第一次中期分析结果在2020 ESMO会议和JCO杂志上同步揭晓。当时公布的中位随访时间是15.5个月,iDFS事件数为323例。此次分析较第一次延长了3.6个月的随访时间,iDFS事件数也达到了395例。
此次中期分析研究结果显示,随着随访时间的延长,患者仍有iDFS的改善,主要终点仍为阳性结果。在次要终点的分析中,Ki67≥20%的人群,iDFS也获得了统计学的改善。这为我们未来临床上辅助治疗使用abemaciclib的人群有很好的提示意义。
在毒副反应方面,我们可以看到该研究毒副反应没有超出预期,腹泻、乏力较常见,而深静脉血栓需关注。接受abemaciclib治疗的患者中,因为不良反应而导致治疗中断的不超过20%,而且大多数患者能耐受。我们非常期待随着进一步随访,这项研究未来能得到总生存的数据,从而把iDFS两年的获益转化为总生存的获益,这是我们对该研究未来的期许。
GS1-02. palbociclib联合内分泌治疗(ET)在激素受体阳性(HR+)、HER2阴性、新辅助化疗(NACT)后高复发风险的原发性乳腺癌患者中的III期研究:PENELOPE-B研究的首次结果
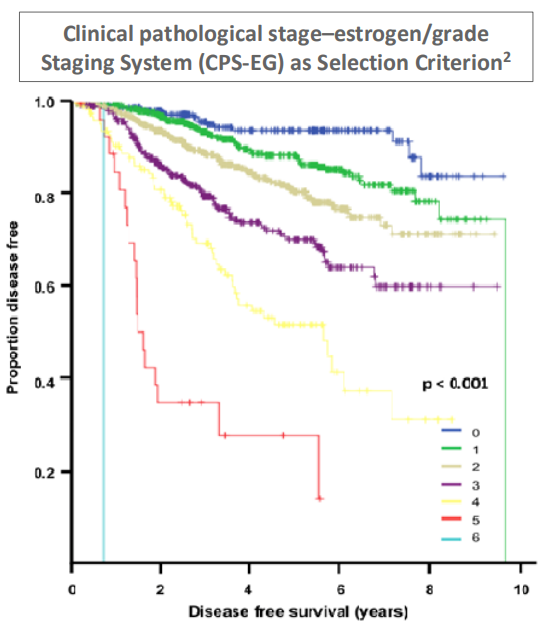
激素受体阳性(HR+)、HER2-原发性乳腺癌新辅助化疗后残留浸润性疾病的患者中,约有三分之一的患者在接受辅助内分泌治疗后仍会复发。使用CPS-EG评分系统可以更准确地评估复发风险(Mittendorf et al. JCO 2011)。palbociclib抑制细胞周期蛋白依赖性激酶4和6(CDK4/6)联合内分泌治疗转移性乳腺癌的疗效显著。因此,我们假设palbociclib可能在这些原发性乳腺癌的高危患者中也有疗效。
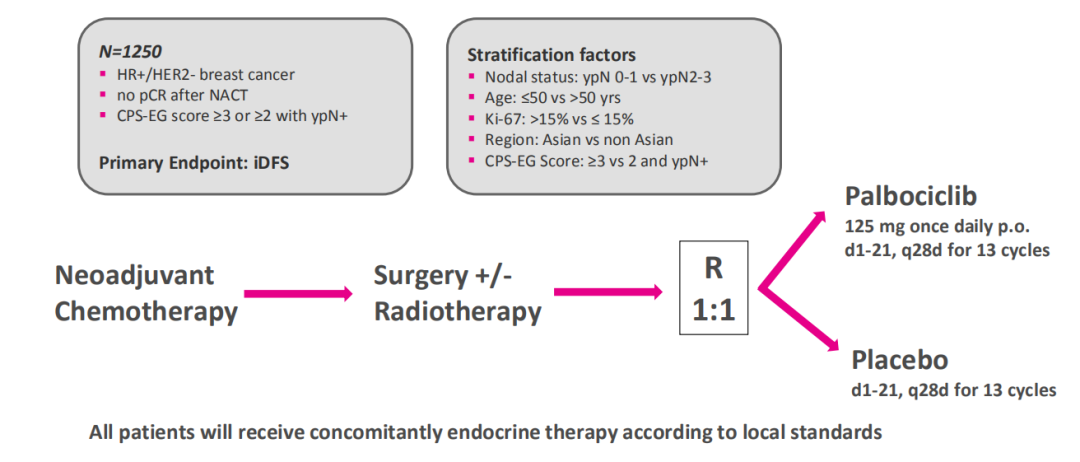
PENELOPE-B(NCT01864746)是一项双盲、安慰剂对照、Ⅲ期研究,研究对象为中心确诊的HR+、HER2-原发乳腺癌患者,在接受含紫杉类的新辅助化疗后未获得病理完全缓解(pCR),且有复发高风险(CPS-EG评分≥3或2且ypN +)。在新辅助化疗和局部区域治疗完成后,除标准内分泌治疗外,患者被随机(1:1)分配到每天接受palbociclib 125mg+ET(palbociclib组)或安慰剂+ET(安慰剂组),每周期28天,在第1-21天接受治疗,共13个周期。根据淋巴结状态(手术时)、年龄、Ki67、全球区域和CPS-EG评分随机分层。主要终点是无侵袭性疾病生存期(iDFS)。基于前两次的中期分析,最终分析计划在290个iDFS事件发生后进行,疗效界值设定为P<0.0463。主要的次要终点包括不包括第二原发侵袭性非乳腺癌的iDFS、总生存率和安全性。
在2014年2月至2017年12月期间,共有1250例患者被随机分组(palbociclib组631例,安慰剂组619例)。患者的中位年龄为49.7岁(范围19-79岁),乳房有残存病灶的占96.8%,ypN+占94.6%,G3占47.4%,Ki67>15%占27.7%,CPS-EG评分≥3的患者为54.7%。1118名患者(89%)完成了至少7个周期的治疗。50.1%的患者接受了芳香化酶抑制剂(AI),49.8%的患者接受了他莫昔芬,6.6%的患者接受了AI+促性腺激素释放激素(GnRH)和9.7%的患者接受了的他莫昔芬+GnRH。最常见的相关严重不良事件(SAEs)是感染和血管疾病,其中报告了8例致命相关严重不良事件。
到目前为止,PENELOPE-B研究的结果不支持在内分泌治疗中增加1年的palbociclib。本次大会公布了相关数据,截止2020年9月25日,中位随访42.8个月,共有308个iDFS事件发生。其中palbociclib组为152个,安慰剂组为156个(HR 0.93,95%CI:0.74~1.17,P=0.525),NACT术后有高危复发风险的HR+/HER2-乳腺癌患者在内分泌治疗中增加1年的palbociclib并没有改善iDFS。预计iDFS发生率:palbociclib组为81.2%,安慰剂组为77.7%;其中远处转移事件发生数为227个(palbociclib组为116个,安慰剂组为111个),占iDFS事件数的74%。
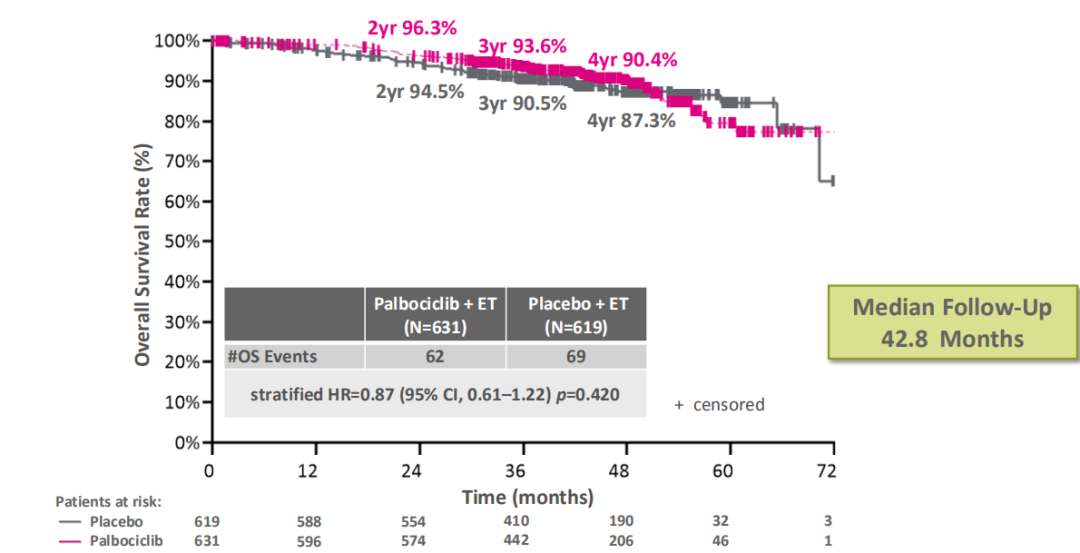
中位随访42.8个月,总生存率(OS)事件数为131个(palbociclib组为62个,安慰剂组为69个(HR 0.87,95%CI:0.61~1.22,P=0.420),两组间无显著差异。
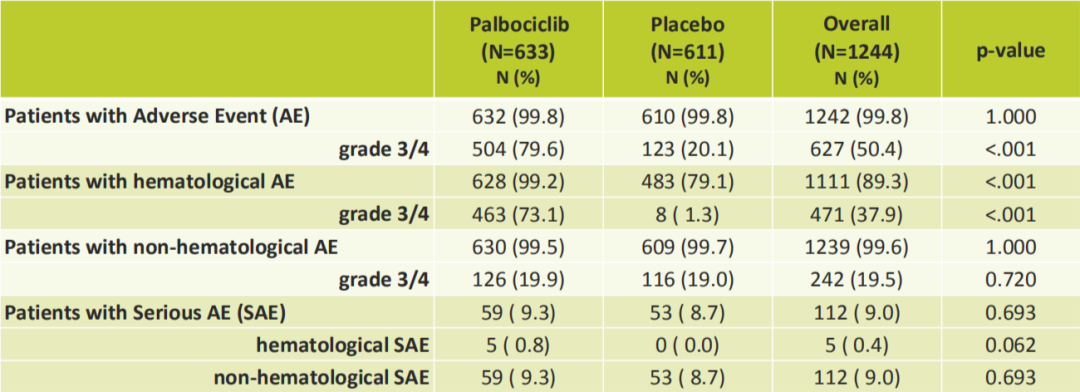
用药依从性方面,palbociclib组低于安慰剂组。不良反应方面,治疗期间无论血液学还是非血液学3~4级不良反应发生率palbociclib组均高于安慰剂组,但没有观察到新的不良反应发生。
这项双盲安慰剂对照的Ⅲ期临床研究,把患者分成了两组,除了在新辅助之后接受标准的内分泌治疗以外,试验组接受了Palbociclib 125毫克口服给药的治疗,用三周停一周,治疗时间为一年。
该研究的iDFS终点之前经过两次期中分析,第一次期中分析中重新校正了样本量和事件数。第二次期中分析是有效-无效性分析,这次是最终分析。在最终分析中,该研究设定了一个名义上的疗效界值P<0.0463,但研究结果显示,没有达到pCR的有高危复发风险(如CPS-EG评分≥3或2伴有淋巴结残留阳性)病人的iDFS,在最终一次随访过程当中(中位随访时间42.8个月),Palbociclib强化组仍然没有达到统计学差异,P值为0.525。
与之前介绍的monarchE研究相比,该研究继续阴性结果的出现可能部分归因于试验设计上的差异,可能是对高危人群筛选的不同,但更有可能是Palbociclib和Abemaciclib两个CDK4/6抑制剂之间本身特性存在不同。PENELOPE-B研究和PALLAS研究的结果都非常令人可惜,从PENELOPE-B亚组分析相关结果来看,似乎暂无一个亚组能够从Palbociclib强化当中获益。这也引起我们的思考,第一,未来我们是不是可以从这两项临床研究中深入挖掘出更合适的人群,或者更高危的人群入组?这是值得我们探讨的。第二,在治疗时间上面,如果有机会把PENELOPE-B研究当中的辅助治疗由一年延长到两年,是不是有机会改变结局?但无论如何,还需要设计新的临床研究去验证这些假设。
GS2-02. 阿那曲唑对比他莫昔芬预防绝经后局部切除导管原位癌女性乳腺癌的12年结果
IBIS-Ⅱ和NSABP B-35两项大型临床试验报告了芳香化酶抑制剂与三苯氧胺(他莫昔芬)对乳腺导管原位癌(DCIS)患者疗效初步分析的不同结果。在这里,我们报告了IBIS-Ⅱ试验12年中位随访疗效和不良事件的数据,该试验比较了阿那曲唑和他莫昔芬在激素受体阳性DCIS患者中的疗效,并关注了治疗后的随访期。
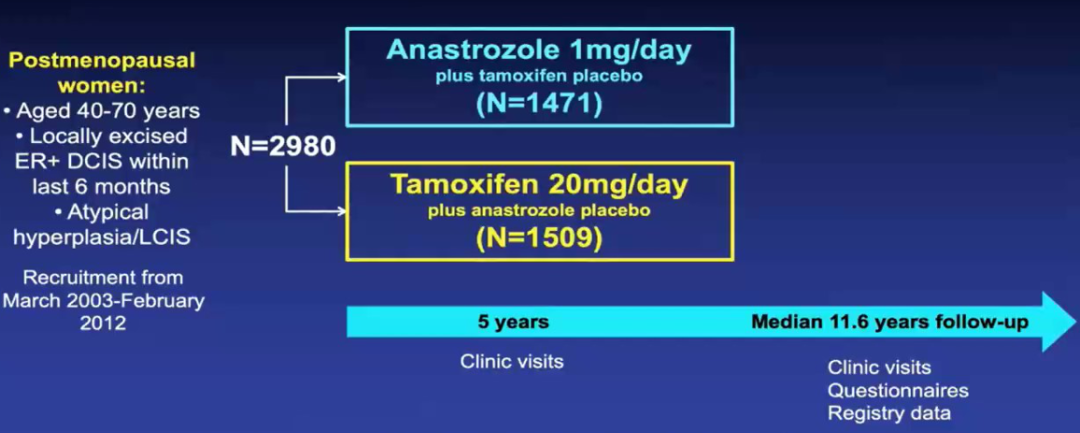
对2003年至2009年间诊断为局部切除的DCIS的绝经后妇女进行了一项为期5年的多中心随机试验,分别接受阿那曲唑1mg/天(N=1471)和他莫昔芬20mg/天(N=1509)。本试验的主要目的是确定阿那曲唑与他莫昔芬在预防复发方面的疗效,尤其是在5年治疗后的随访期间。次要终点包括复发类型、乳腺癌死亡率、其他癌症、心血管疾病、骨折、不良事件和非乳腺癌死亡。
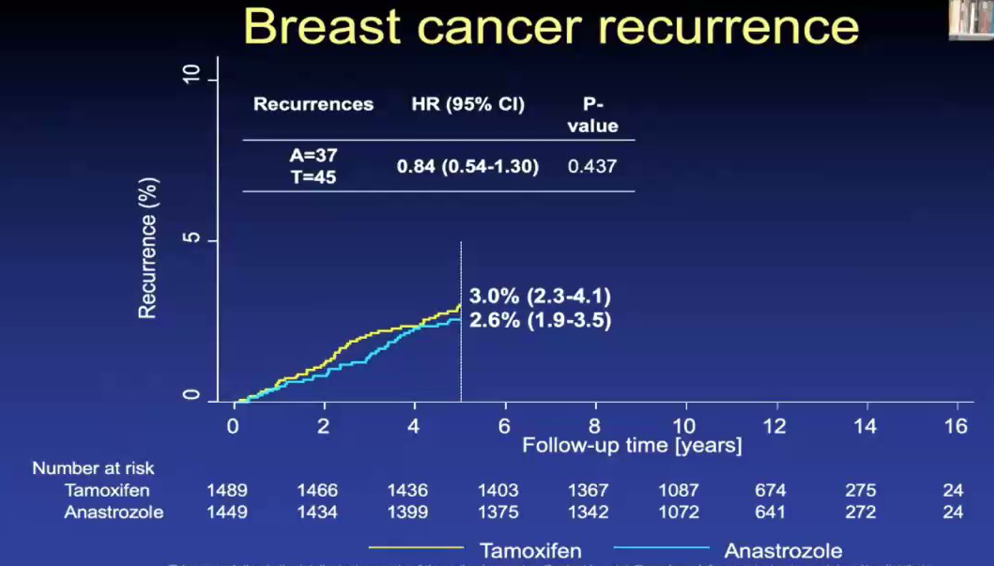
中位随访11.6年(IQR 9.9至13.4)后,共记录了221例乳腺癌复发(7.4%)。在5年治疗期 (HR=0.82(0.53~1.27),P=0.37),或治疗后随访期(HR=0.91,95%CI:0.65~1.27,P=0.57),阿那曲唑对比他莫昔芬组总体复发率没有差异,阿那曲唑组和他莫昔芬组分别有102例 (6.9%)和119 例(7.9%)乳腺癌复发(HR=0.87,95%CI:0.67~1.14,P=0.32)。与他莫昔芬相比,使用阿那曲唑的雌激素受体(ER)阳性乳腺癌减少了28%(58例 vs.82例;HR=0.72,95%CI:0.52~1.01,P=0.056),但并未达到显著水平。
相反,阿那曲唑对ER阴性乳腺癌没有观察到有疗效。与他莫昔芬相比,阿那曲唑在减少浸润性乳腺癌复发方面没有显著差异。与他莫昔芬相比,阿那曲唑对浸润性ER阳性乳腺癌的疗效无显著性降低24%(44例 vs.59例;HR=0.76,95%CI:0.51~1.12)P=0.17)。共报告了127例死亡,两种治疗方法的全因死亡率无显著差异(61例vs.66例;HR=0.94,95%CI:0.67~1.33,P=0.74)。只有7例死于乳腺癌(3例 vs.4例),随访到12年时死于乳腺癌的人数很少,对生存率的影响不太可能通过更长时间的随访而显现。报告214例乳腺癌以外的癌症,使用阿那曲唑观察到无显著性降低(97例 vs.117例,OR=0.84,95%CI:0.63~1.12,P=0.22)。阿那曲唑治疗子宫内膜癌(2例vs.13例,OR=0.16,95%CI:0.02~0.0.69)、卵巢癌(1例vs.9例,OR=0.11,95%CI:0.003~0.82)和非黑色素瘤皮肤癌(11例vs.21例)较少见。与他莫昔芬相比,阿那曲唑组的骨折发生率(181例vs.145例,OR=1.32,95%CI:1.04~1.68)和短暂性缺血发作(15例vs.5例,OR=3.10,95%CI:1.07~10.92)显著增高。未来将报告全面的不良事件概况。
该项研究是IBIS-Ⅱ临床研究的进一步随访结果。IBIS-Ⅱ和NSABP B-35都是探索芳香化酶抑制剂和他莫昔芬对照在DCIS患者当中的疗效的研究,但它们的结果却有所不同,在NSABP B-35中有阳性的结果,阿那曲唑获益要多一点,而在IBIS-Ⅱ临床研究当中,却没有看到大的差异。
本次大会报告是随访12年之后的再次疗效分析,结果发现,在中位随访11.6年,共记录到221例乳腺癌复发,同时发现在阿那曲唑治疗组与他莫昔芬治疗组相比,在总体的复发率上面没有太大的差异。即复发风险上有一定绝对值和相对值的下降,但是未达到显著水平。死亡风险也没有下降。NSABP B-35中阿那曲唑的远期效应没有在IBIS-Ⅱ临床研究观察到。
经过将近12年的随访,同样也看到了在一些其他特征上的差别,如非乳腺癌的肿瘤发生,包括子宫内膜癌、卵巢癌等,阿那曲唑组更少。但是阿那曲唑组的骨折发生率和短暂性脑缺血发作(TIA)/卒中却更高。
该项临床研究长期随访的结果带给我们的启示:我们在DCIS患者后续治疗时,可能更关注的是患者的整体耐受性。如果患者在使用AI治疗过程中耐受性是可以的,我们完全可以继续使用AI进行预防ER+乳腺癌。但如果不耐受,使用他莫昔芬完全也是可以的。二者从预防终点事件上面来讲,是没有太大差别的。毒副反应、疗效、费用三方面是我们临床决策需要考虑的问题。
总而言之,12年随访的结果与IBIS-Ⅱ前几次分析的结果是一致的,AI和他莫昔芬都是我们临床当中重要的选择。
?





 京公网安备 11010502033352号
京公网安备 11010502033352号