编者按:一年一度的美国临床肿瘤学会年会(2020 ASCO)于线上成功举办,乳腺癌领域进展不断,一副长卷徐徐展开。为尽快让国内乳腺领域专家学者领略ASCO进展的风采,6月11日,“HER燃新声”直播间直击前沿,速递进展,复旦大学附属肿瘤医院邵志敏教授坐镇主场,复旦大学附属肿瘤医院李俊杰教授、张剑教授共同主持,复旦大学附属肿瘤医院杨犇龙教授、大连医科大学附属第二医院徐岭植教授分别分享 ASCO早期及晚期乳腺癌治疗新进展,众多中青年才俊做客直播间,挥毫泼墨,展开深入讨论,就ASCO最新前沿动态及相关报告内容传播分享,洞察己见,给您带来不一样的观感。
HER燃新声,中青年才俊为您带来最前沿的学术美景。直播在邵志敏教授的对青年医生的谆谆寄托下拉开帷幕,希望年轻医生能够紧跟前沿进展,学习、分享、讨论和提高。随后李俊杰教授、张剑教授共同主持介绍了此次与会的专家及日程,为我们徐徐展开一幅学术长卷。
随着靶向药物的发展,HER2阳性乳腺癌的治疗有了长足的进步。然而70%以上的患者仅通过曲妥珠单抗联合化疗即可求得8-10年的无病生存,面对更多的武器应如何选择最优的策略?T-DM1的患者如何选取?KATHERINE研究的生物标志物数据研究针对早期HER2阳性乳腺癌患者新辅后残余病灶抗HER2升阶治疗生物标记物与iDFS关系进行探索,该研究中80%的标本为新辅助治疗后的标本。结果显示各个生物标志物亚组中T-DM1均取得了绝对优势,而高HER2表达与曲妥珠单抗组的预后不良相关,提示新辅抗HER2治疗后的高HER2表达可能和曲妥耐药机制有关,而TDM-1组不受影响意味着它可能能克服这种耐药机制。
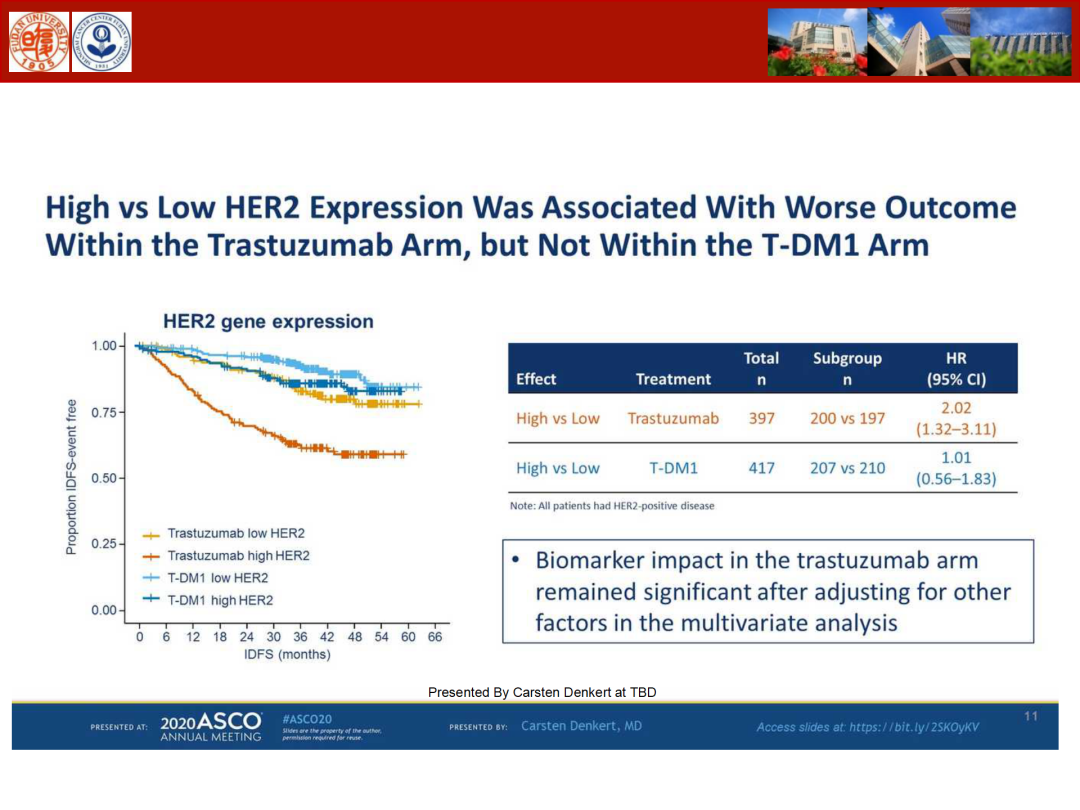
那么T-DM1是否可以取代紫杉类?KAITLIN研究对高危患者分别在蒽环治疗后予以妥妥双靶联合紫杉vs T-DM1联合帕妥珠单抗,结果显示二者并无显著差异,T-DM1的优势人群需要进一步探寻。
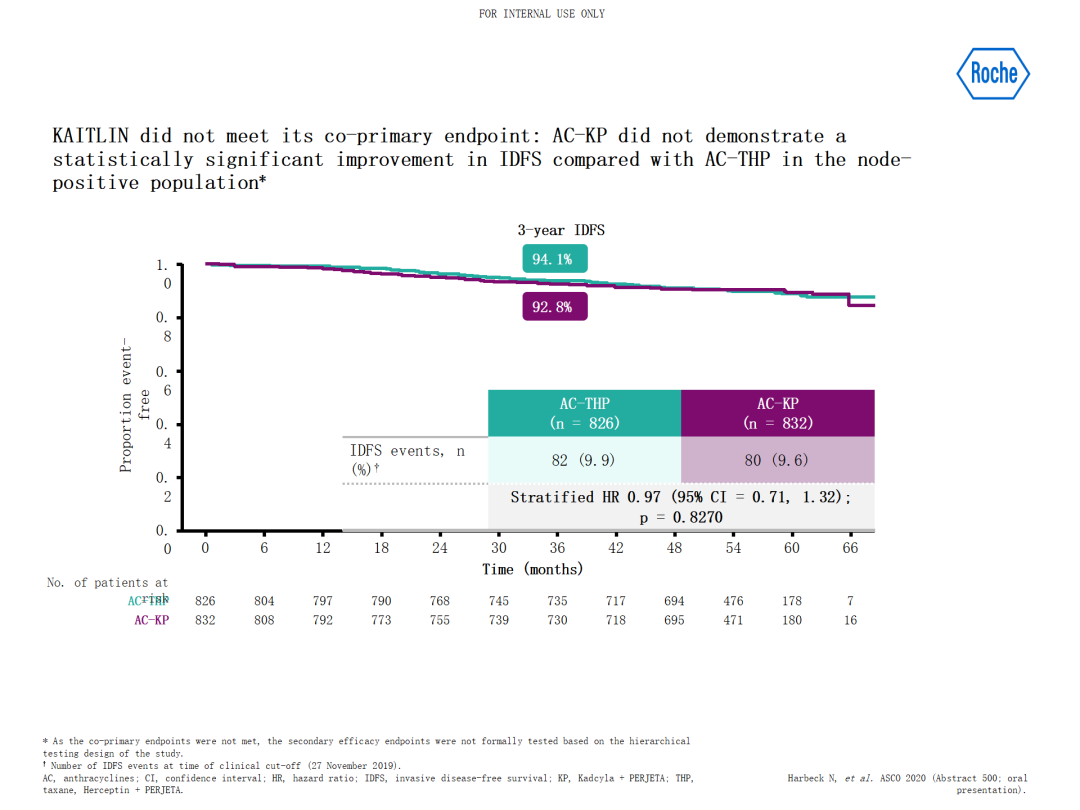
KAITLIN研究中患者均使用蒽环类药物,蒽环是否是必须品?TRAIN-2研究对比了9周期TCbHP与3周期FEC-T联合帕妥珠单抗+6周期TCbHP的疗效与安全性,结果显示二者EFS、OS均无显著差异,蒽环组反而有更高的心脏毒性,因此TCbHP更为可靠,蒽环的选择需要精准医疗的介入来判断去留。
蒽环可去,化疗可免否?PHERGAIN研究通过多臂设计使用PEC-CT评估疗效以决定方案调整给了临床指导思路。结果显示,PET-CT无反应组,即使加用化疗,pCR率仍较低于反应组,而TCbH组若PET-CT无反应,则pCR率仅为10%,提示方案需要尽早转换,PET-CT为患者更换方案、去化疗提供了指导思路。

MINDACT研究对70基因检测指导辅助治疗的8年结果进行了公布,提示根据年龄分层,≤50岁的临床高危、基因低危患者加用化疗可以提高患者获益。因此,70基因对于年龄超过50岁患者豁免化疗具有指导意义。
ALERNATE研究以疾病内分泌治疗敏感率(ESDR)为研究终点,即mPEPI 0(pT1/2 pN0, Ki67≤2.7%,ER Allred 3-8)与pCR率之和,判断三种新辅助内分泌治疗的疗效,虽然方案非CDK4/6抑制剂时代的首选,结果也为阴性,但ESDR作为评判指标是可行的。FELINE研究则在新辅助内分泌治疗基础上加用了CDK4/6抑制剂,显示并未增加手术前PEPI0的比例,差异亦不明显,需要进一步探索联合用药的可行性。
NSABP-43研究报告了HER2阳性DCIS患者肿块切除术后辅助治疗选择常规乳腺放疗基础上加入曲妥珠单抗治疗对比单纯放疗预防同侧乳腺癌、皮肤恶性肿瘤和DCIS等(统称IBTR)。在RT中添加曲妥珠单抗并没有达到IBTR率降低36%的预设目标,虽有改善但仍是阴性结果,所以抗HER2治疗对DCIS的升阶梯仍需探索。
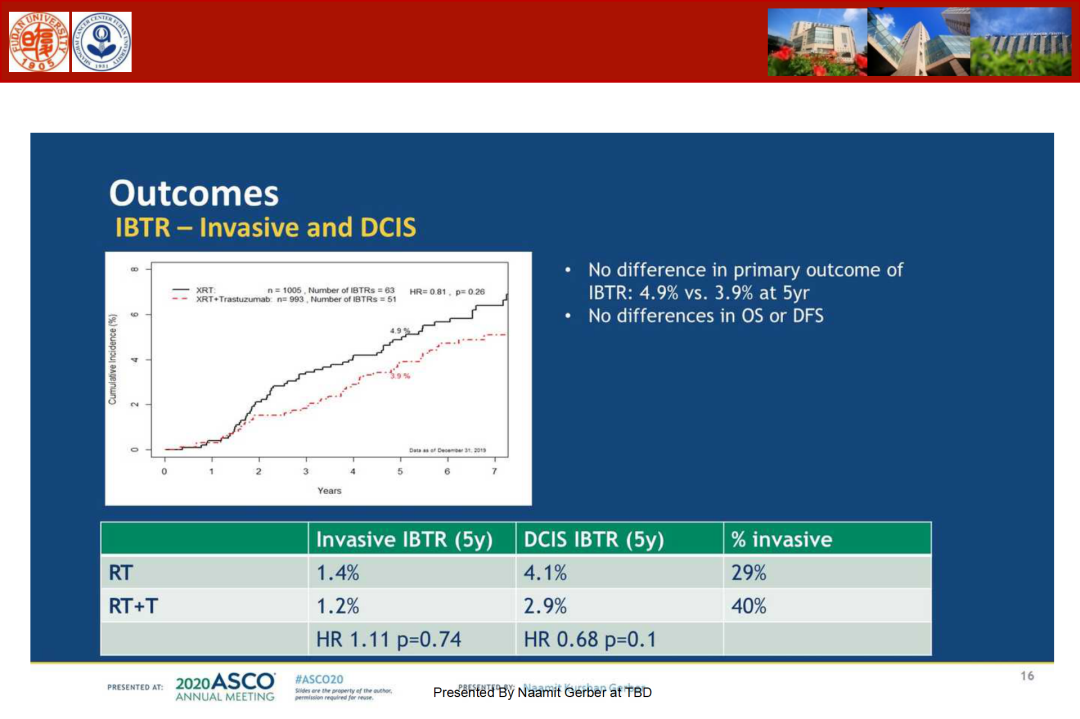
我国的SYSUCC-001研究讨论了对可手术TNBC患者卡培他滨节拍化疗的价值,DFS仅取得10%的获益,OS未见显著差异,结果不甚理想。结合三阴乳腺癌的混杂性以及化疗方案的局限性,卡培他滨在TNBC的地位仍需谨慎考量,需要在未来进一步进行精准探索,确定适宜人群。
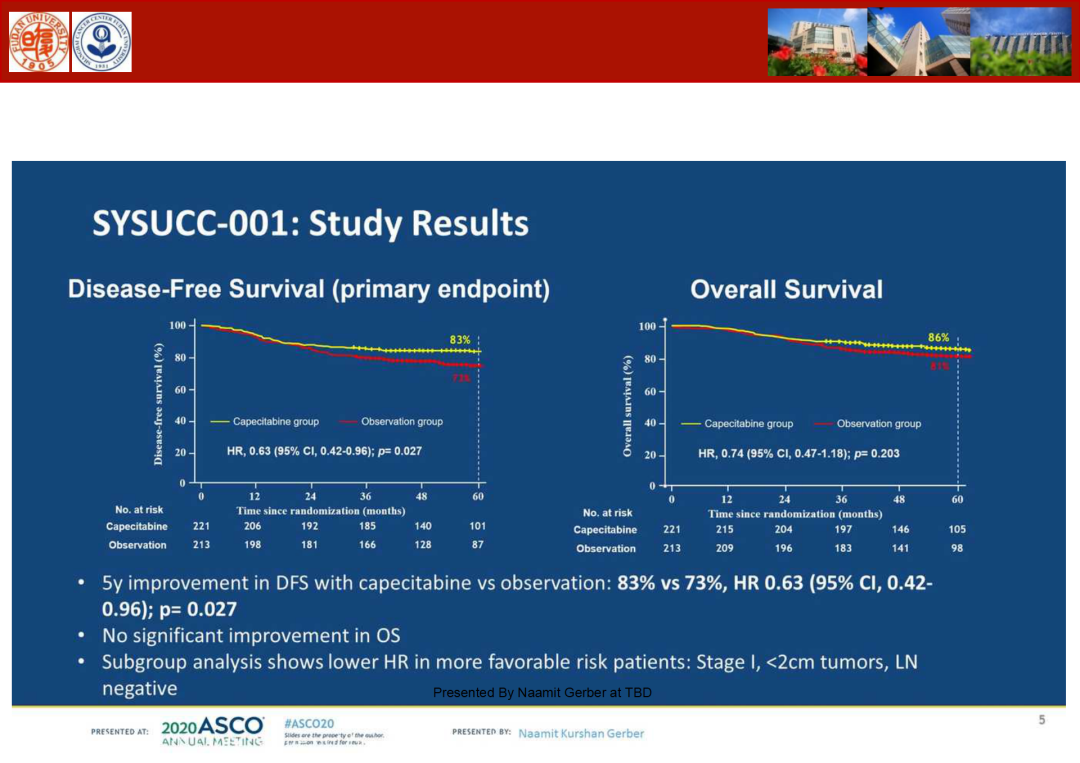
在杨犇龙教授分享了ASCO早期乳腺癌进展之后,五位青年才俊从不同角度对早期乳腺癌诊疗进展进行深入探讨,邵志敏教授小结点评,为这一卷画面再添生动。
朱丽教授
相对其他新辅助治疗降期保乳的目的,新辅助内分泌治疗的主要目的是筛选可豁免化疗的患者。ALERNATE、FELINE研究显示了在激素受体阳性,HER2阴性患者中,AI类药物的强势地位,CDK4/6抑制剂的增加并无显著优势。此外,在三阳性患者中,内分泌联合抗HER2靶向治疗也是探索的方向。但新辅助内分泌治疗仍处于临床探索阶段,免化疗仍需谨慎。
HER2阳性乳腺新辅助治疗目前已经是闭环式管理模式:化疗降阶、靶向升阶及术后强化。化疗降阶一是减少化疗药物的数量,二是去蒽环药,三是能否免除化疗药;在妥妥双靶前提下减少化疗的数量已经是毋庸置疑的了;而通过KRISTINE及KAITLIN两项研究证实了免除化疗还为时过早;目前的争论主要集中在去蒽环方面,AC-THP与TCbHP在pCR率方面并没有太大的差异;支持去蒽环药的原因:有蒽环一是不能尽早的的应用妥妥双靶,二是会增加心脏的毒副作用;不支持去蒽环药的原因:就是在辅助治疗中临床数据更支持含蒽环类的方案,尤其在BCIRG006研究中表明TOP2A基因扩增者靶向及TCbH治疗效果不佳,含蒽环药的方案更获益;因此,目前去蒽环仍需谨慎。其实,AC-THP及TCbHP这两种方案并不是誓不两立、非此即彼,更应该是互相补充、相辅相成的,因为对于新辅助Non-pCR者在术后还有T-DM1的强化治疗。虽然KATHERINE研究中80%入组的都是单靶治疗的,很多专家认为妥妥双靶治疗之后的Non-pCR后用T-DM1去强化治疗的数据并不充分。但这次ASCO会议中关于KATHERINE实验中肿瘤标志物的研究表明在术后标本中HER2蛋白强表达者更适合T-DM1治疗,也就说T-DM1更适合抗HER2耐药或不敏感者,在亚组分析中也可以看到术后残留病灶越大者T-DM1越获益。越来越多的抗HER2药物的问世,使HER2+这类乳腺癌与HR+亚型相似,也会变成一种慢性病,所以抗HER2治疗更要精打细算、精益求精地去排兵布阵。
KATHERINE研究分析了生物标志物的预测及预后价值,发现新辅助后HER2高表达患者辅助应用曲妥珠单抗治疗预后差,而辅助T-DM1治疗组不受HER2表达高低影响。潜在说明在新辅助治疗中对抗HER2治疗不敏感的患者对T-DM1反应好,提示HER2高表达可作为后续T-DM1治疗的疗效预测指标。今年ASCO会议中很多研究试图探索HER2阳性乳腺癌的降阶梯治疗,KAITLIN研究旨在比较T-DM1能否替代传统紫杉,虽以阴性结果告终,但我们看到对于高危人群,妥妥双靶联合治疗3年iDFS依然可达93-94%。随着抗HER2治疗的强化,未来新辅助平台可能为辅助降阶治疗提供更多依据。
从TAILORx到MINDACT研究,基因检测对临床方案的指导愈加重要,尤其是对于年龄50岁为分界线的患者更具有指导意义,但其研究纳入的风险因素有限,需要进一步拓展验证,所以目前辅助治疗仍需以临床风险因素为主要评判,如年龄、肿瘤大小、淋巴结转移、脉管癌栓等。
TNBC使用卡培他滨辅助治疗在SYSUCC-001研究并未取得OS获益,但DFS风险有显著降低,而且在肿瘤负荷较低的患者中,患者获益更多,其原因仍需进一步验证。但对于TNBC患者而言,卡培他滨辅助治疗仍是当前优选的方案之一。
今年ASCO带来了很多思考,比如三阴性乳腺癌未来的发展将会是基于基因分型下的精准治疗,将会在未来的指南中有明确体现。另外,基于PHERGAIN研究,新辅助治疗早期评估和决策的概念非常重要,是否需要完成新辅助治疗所有周期是值得推敲的,需要完整的SOP指导。





 京公网安备 11010502033352号
京公网安备 11010502033352号